Notre plateforme NANOp2Lysis®
La plateforme NANOp2Lysis® combine une technologie de vectorisation de rupture, un savoir-faire industriel permettant le scale up vers des productions de qualité clinique, et un savoir-faire et une expertise préclinique incluant la mise en place de modèles prédictifs et translationnels, une première dans ce domaine.

Cette technologie permet de réduire le nombre d'injections et les doses utilisées.
La plateforme NANOp2Lysis® permet la vectorisation de molécules biologiques pour assurer une action plus efficace. La molécule biologique est nanoprécipitée puis encapsulée dans un polymère assurant une haute protection de la molécule biologique pendant le transport vers le tissu ciblé et une libération graduelle adaptée. Ainsi, la technologie NANOp2Lysis® dévoile toute l’efficacité des principes actifs permettant de réduire le nombre d’injection et la dose utilisée.
Le choix du polymère est guidé par l’indication et la cible du traitement thrombolytique.
Une technologie d'administration unique préservant la structure 3D de la molécule biologique
Un problème critique avec les agents thrombolytiques (capable de dégrader les thrombus) est leur faible demi-vie dans la circulation, nécessitant de multiplier la fréquence des injections. La technologie de libération prolongée offre la promesse de réduire la fréquence des injections, de maximiser la relation efficacité-dose et de diminuer les effets secondaires indésirables.
Cependant, formuler et vectoriser des agents thrombolytiques afin d’obtenir une libération prolongée est complexe car la plupart des processus de fabrication provoquent la dénaturation de ces agents. La technologie propriétaire NANOp2Lysis® permet de résoudre cette complexité et d’encapsuler des agents thrombolytiques actifs dans des systèmes polymériques pour obtenir une libération prolongée avec un haut rendement.
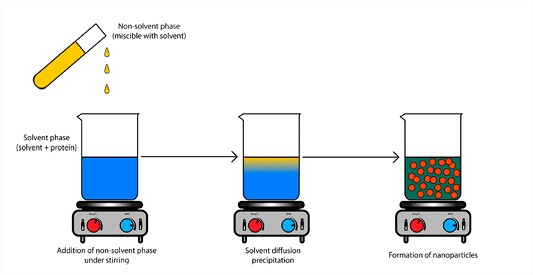
Une technologie robuste et adaptable pour alimenter un pipeline de produits
La technologie de nanoprécipitation de la plateforme NANOp2Lysis® est une technique robuste, répétable et industrialisée. Les nanoparticules solides d’OptPA obtenus avec cette technologie peuvent être intégrés dans divers polymères pour répondre aux spécificités des indications traitées. NANOp2Lysis® constitue une approche de médecine personnalisée et une opportunité de développer un pipeline de produits complémentaires pour tous les AVC hémorragiques et au-delà.
OPTPA
Un agent thrombolytique plus sûr
Les agents thrombolytiques de la famille des « activateurs du plasminogène » activent le plasminogène, une proenzyme endogène inactive, en plasmine, une forme active qui décompose la trame de fibrine constituant le caillot sanguin permettant ainsi sa dégradation. C’est pour cette raison que le tPA a été développé comme médicament au début des années 80 pour traiter les maladies cardiaques et les accidents vasculaires cérébraux ischémiques (années 90). Aujourd’hui encore, la thérapie thrombolytique offre plusieurs avantages, notamment un bon rapport coût-efficacité et une utilisation dans n’importe quel hôpital.
Cependant, de nombreux effets secondaires ont également été décrits lors de l’administration de tPA dans le traitement de l’accident vasculaire cérébral ischémique, notamment un risque accru de transformation hémorragique. Expérimentalement, de nombreux groupes ont démontré un rôle excitotoxique et inflammatoire du tPA dans le traitement de l’AVC.
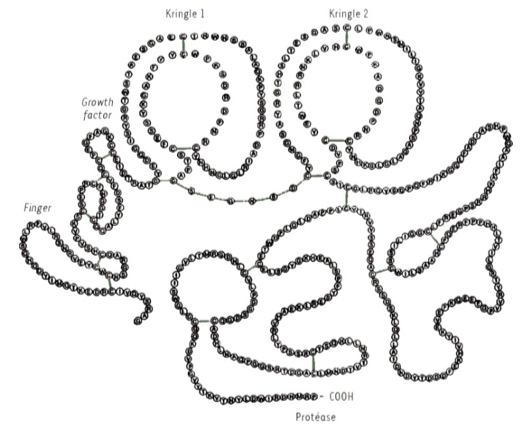
Le tPA optimisé (OptPA), breveté, a été conçu à partir de ces observations. OptPA est un variant du tPA contenant deux mutations ponctuelles, (1) le remplacement du tryptophane par l’arginine en position 253 et (2) le remplacement de l’arginine par la sérine en position 275. Du fait de ces mutations, OptPA est dépourvu des effets secondaires décrits ci-dessus, tout en conservant une activité thrombolytique élevée. L’OptPA a un meilleur profil de sécurité est plus sûr tPA.
RÉFÉRENCES
Thiebaut A. M., Louet E. R., Ianszen M., Guichard M-J, Hanley D.F., Gaudin C., Parcq J. (2023). O2L-001, an innovative thrombolytic to evacuate intracerebral haematoma. Brain, 146(11):4690-4701.
doi: 10.1093/brain/awad237.
Goulay, R., Naveau, M., Gaberel, T., Vivien, D., & Parcq, J. (2018). Optimized tPA: A non-neurotoxic fibrinolytic agent for the drainage of intracerebral hemorrhages. Journal of Cerebral Blood Flow & Metabolism, 38(7), 1180–1189.
Parcq, J., Bertrand, T., Baron, A. F., Hommet, Y., Anglès-Cano, E., & Vivien, D. (2013). Molecular requirements for safer generation of thrombolytics by bioengineering the tissue-type plasminogen activator A chain. Journal of Thrombosis and Haemostasis, 11(3), 539–546.
Giteau, A., Venier-Julienne, M.-C., Marchal, S., Courthaudon, J.-L., Sergent, M., Montero-Menei, C., Verdier, J.-M., & Benoit, J.-P. (2008). Reversible protein precipitation to ensure stability during encapsulation within PLGA microspheres. European Journal of Pharmaceutics and Biopharmaceutics, 70(1), 127–136.
Paillard-Giteau, A., Tran, V. T., Thomas, O., Garric, X., Coudane, J., Marchal, S., Chourpa, I., Benoît, J. P., Montero-Menei, C. N., & Venier-Julienne, M. C. (2010). Effect of various additives and polymers on lysozyme release from PLGA microspheres prepared by an s/o/w emulsion technique. European Journal of Pharmaceutics and Biopharmaceutics, 75(2), 128–136.